La Agencia Española de Medicamentos y Productos Sanitarios (Aemps), dependiente del Ministerio de Salud de España, autorizó este miércoles el primer ensayo clínico de la primera vacuna española contra el Covid-19 con personas voluntarias entre 18 y 39 años, según reportó la agencia local Cadenaser.
Se trata de una vacuna de proteína recombinante, fue desarrollada por la compañía farmacéutica Hipra con el nombre provisional PHH-1V. Según proyecciones actuales de la empresa está prevista que se produzca 400 millones de dosis durante el año 2022.
Para el 2023 se podrían alcanzar los 1.200 millones de dosis. La compañía también está llevando a cabo otra línea de investigación en colaboración con el Hospital Clínica de Barcelona para el desarrollo de una vacuna contra el coronavirus.
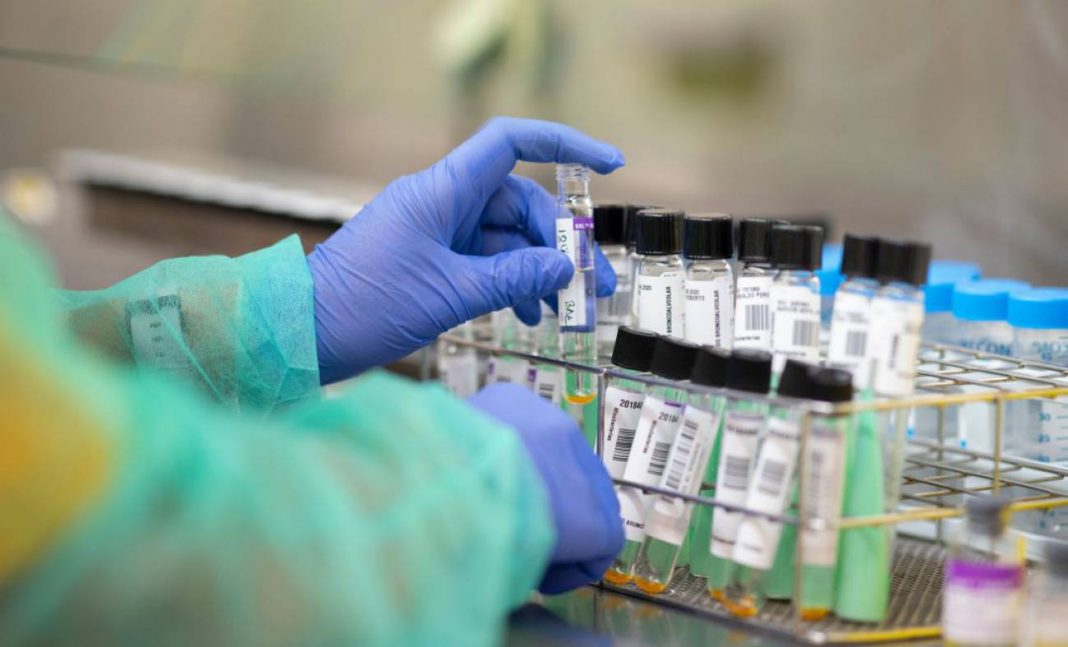
En esta primera fase del ensayo clínico en humanos, participarán varias decenas de voluntarios, el objetivo es analizar la seguridad y la tolerancia de este candidato a vacuna. Cada participante, recibirá dos dosis de este inmunizante separadas por 21 días.
Tecnología de la vacuna
Esta vacuna está basada en dos proteínas recombinantes y se puede guardar a tan solo dos grados de temperatura. Estos albuminoides son estructuralmente similares, una correspondiente a la variante alfa y otra a la variante beta, que se unen formando una estructura única llamada dímero.
Esta combinación es capaz de generar una respuesta inmunológica frente a una de las proteínas del virus, conocida como proteína S (de spike, también llamada proteína espiga en español). Este sistema es el mismo que se ha utilizado para las vacunas Novavax y Sanofi / GSK, que ya están en proceso de evaluación para su potencial autorización por parte de la Agencia Europea del Medicamento, pero a diferencia de ellas, expresa proteínas de dos variantes distintas.
/GFS/